- Katı:Katılarda moleküller yapı boyunca tekrarlayan bir düzende dizilir.
- Sıvılarda:moleküllerin birbirlerine göre konumları sabit olarak kalmaz ve bunlar serbestçe dönüp yer değiştirebilir.
- Gaz:moleküller birbirlerinden oldukça uzaktadır ve moleküller arasında bir düzenden söz edilemez.
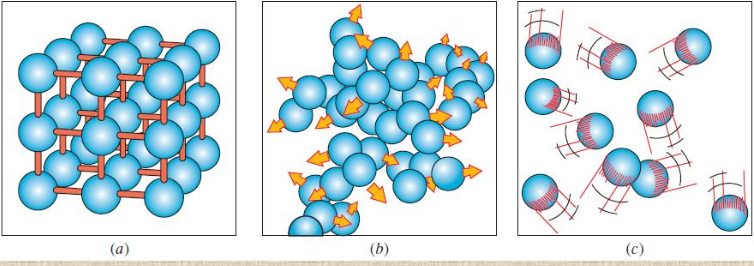
Maddenin farklı fazlarındaki atom düzenleri: (a) katılarda moleküllerin konumları sabit, (b) sıvılarda molekül grupları halinde, (c) gazlarda ise moleküller gelişigüzel hareket eder.
Gaz vebuhar sözcükleri çoğunlukla birbirleri yerine kullanılır. Gaz:Bir maddenin buhar fazı, genellikle kritik bir sıcaklığın üzerinde ise gaz olarak adlandırılır.Buhar:Bu terim genellikle yoğuşma koşullarına çok yakın bir gaz halini ifade eder.
Makroskobik veyaklasikyaklaşım:Her bir molekülün davranışının bilinmesine ihtiyaç yoktur ve bu yaklaşım mühendislik problemlerinin doğrudan ve kolaylıkla çözülebilmesine olanak sağlar. •Mikroskobikveyaistatistikselyaklaşım:Moleküllerin bir araya gelerek oluşturdukları büyük molekül gruplarının davranışını esas alır.
Mikroskobik bir ölçekte bir gazın basıncı gaz moleküllerinin etkileşimine dayalı olarak belirlenirken, makroskobik ölçekte bir manometre ile ölçülebilir.
Alıntı: Akışkanlar Mekaniği: Temelleri ve Uygulamaları3’üncü Baskıdan ÇeviriYunus A. Cengel, John M. CimbalaMcGraw-Hill, 2014
Link: http://personel.klu.edu.tr/dosyalar/kullanicilar/utkuyilmaz/dosyalar/dosya_ve_belgeler/akm_cengel_dn_bolum_01.pdf
